考试题目
一、脑膜瘤
1.临床
多见于中年女性
起源于蛛网膜粒帽细胞,多在脑外,与硬脑膜粘连。好发部位为矢状窦旁、大脑凸面、桥小脑角、大脑镰或小脑幕等处。包膜完整,血供丰富,多有钙化,少有出血、坏死、囊变。WHO 1级:脑膜瘤,WHO 2级:非典型性脑膜瘤,WHO 3级:间变型脑膜瘤
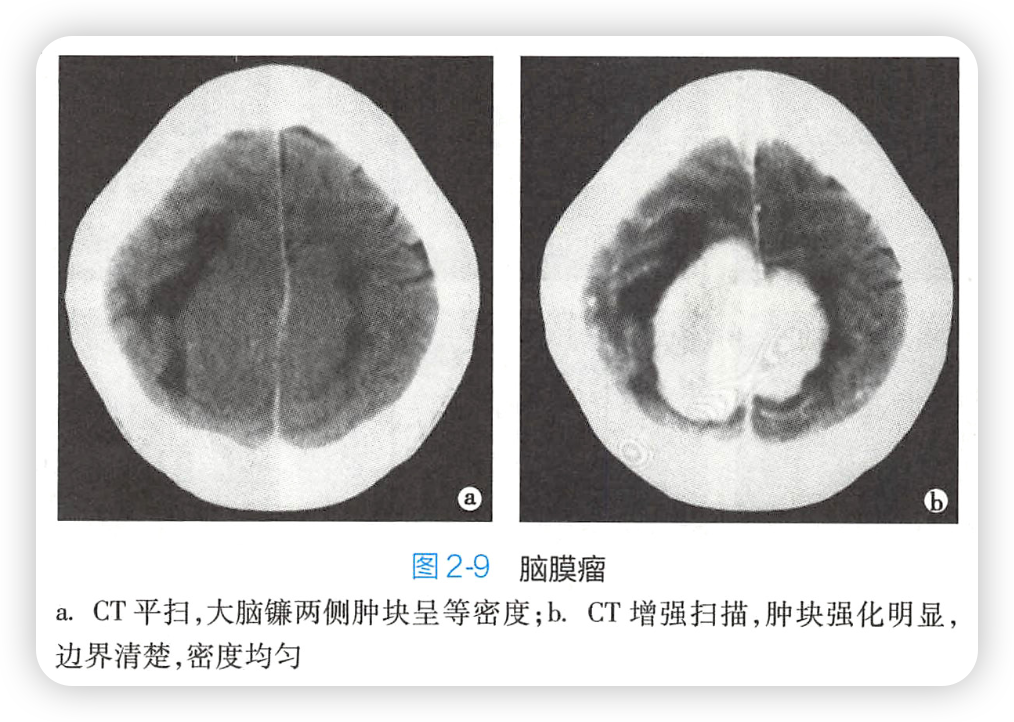
2.影像
1)CT:
(1)平扫,类圆形肿块等/高密度,边界清楚,内部常见斑点状钙化
(2)多以广基底与硬脑膜相连
(3)瘤周水肿轻/无,静脉受压可有中/重水肿
(4)颅板受累,局部骨质增生/破坏
(5)增强,多均匀显著强化
2)MRI:
(1)多在脑实质外,T1WI等/稍高,T2WI等/高,高级别脑膜瘤常坏死、囊变
(2)增强T1WI,1级均匀显著强化,2/3级斑片状不均匀强化并侵犯组织。
脑膜尾征:临近脑膜增厚并强化。
(3)MRA,明确静脉压迫程度、内部有无血栓
二、星形细胞瘤
1.临床
中枢神经系统最常见,起源于神经上皮组织。成人多大脑,儿童多小脑。病变多在白质。
按分化程度不同分为1~4级:
1级分化良好、低度恶性,
2级良恶性之间,
3~4级分化不良,高度恶性。
2~4级浸润性生长,分界不清,易坏死、出血。
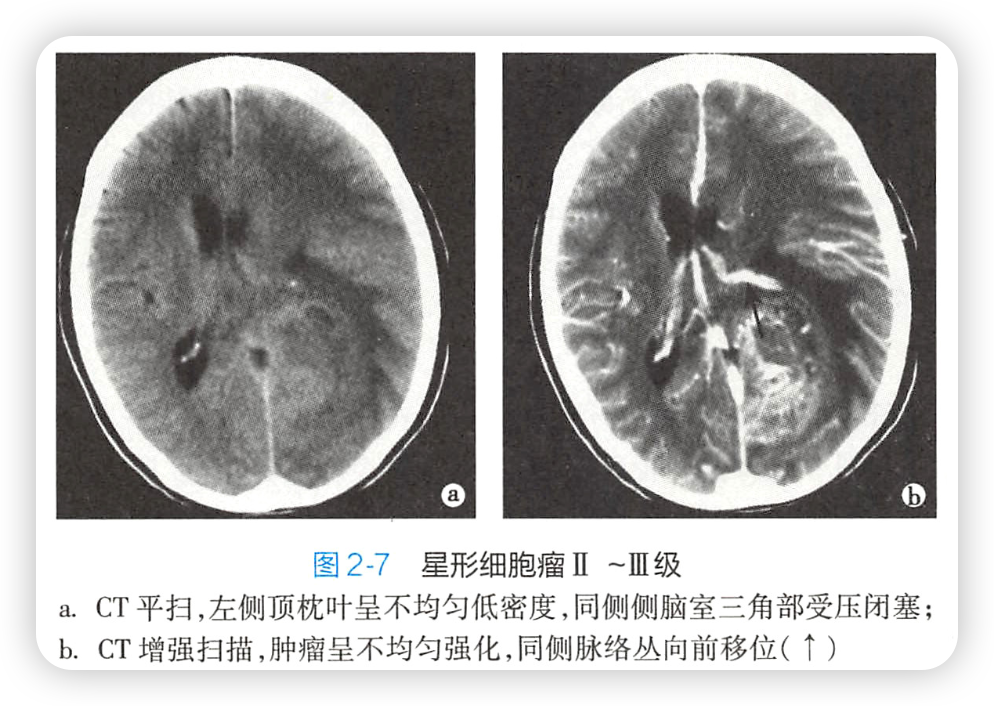
2.影像
1)CT
1级肿瘤:
(1)平扫,低密度灶,边界清楚,占位效应轻
(2)增强,绝大多数无/轻度强化(除毛细胞型、室管膜下巨细胞型)
2~4级肿瘤:
(1)平扫,形态不规则的高/低/混杂密度肿块,可有出血、斑点状钙化
(2)边界不清,占位效应、瘤周水肿明显
(3)增强,2级多无/轻度强化,3、4级多明显强化,少数无强化
2)MRI
(1)T1WI稍低/混杂信号,T2WI(不)均匀高信号
(2)增强,与CT增强扫描类似(增强T1WI,4级花环样强化)
(3)DWI,恶性越高,ADC值越低
(4)MRS
(5)PWI
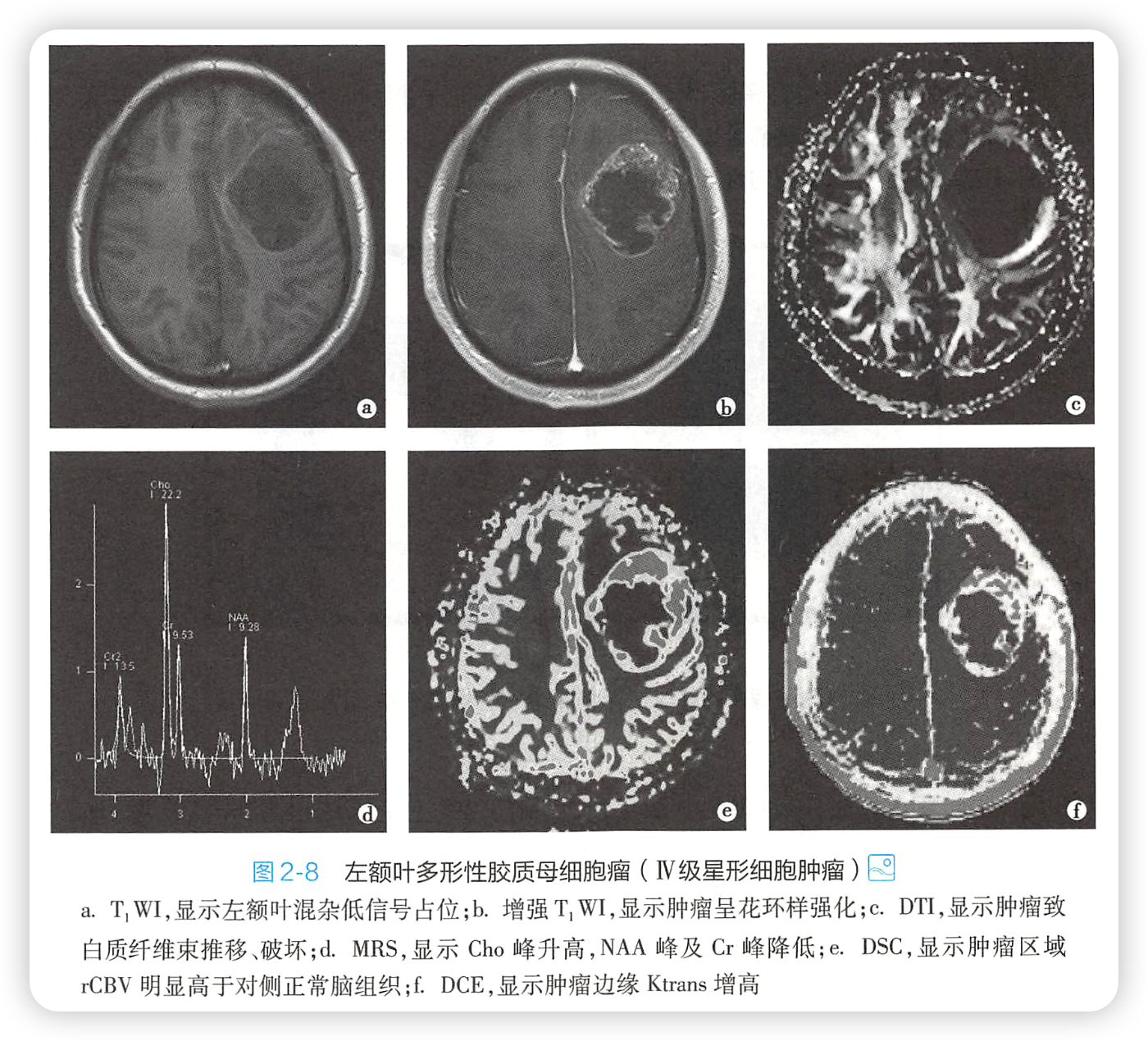
三、脑脓肿
1.临床:耳源性多见,多发于颞叶、小脑。
2.影像
1)CT
急性炎症期:
(1)平扫,大片低密度灶,边界不清,占位效应;
(2)增强,无强化或不规则斑点状、脑回样强化
化脓坏死期:
(1)平扫,低密度区内有更低密度坏死灶
(2)增强,不均匀轻度强化
脓肿形成期:
(1)平扫,等密度环,内有低密度并可见气泡影
(2)增强,环形强化(脓肿壁),完整、光滑、均匀
2)MRI
急性炎症期:
(1)T1WI稍低,T2WI稍高,边界不清,占位效应明显
(2)增强,无强化或斑点状不均匀强化
化脓坏死期:
(1)病灶内出现T1更低信号区,T2高信号;周边T1等/稍高,T2等的不规则薄壁
(2)增强,薄壁不规则环状强化
脓肿形成期:
(1)脓肿壁T1等/稍高,T2稍低/等。脓液T1低,T2高
(2)DWI,脓腔内明显高信号
(3)增强,光滑薄壁环形强化
四、脑外伤
1.临床
脑挫裂伤、脑内出血、脑外出血(硬膜外、硬膜下、蛛网膜下腔)
2.影像
1)CT
脑挫裂伤:
(1)平扫,低密度脑水肿,斑点状高密度出血灶。可广泛性脑水肿、脑内血肿
硬膜外血肿:
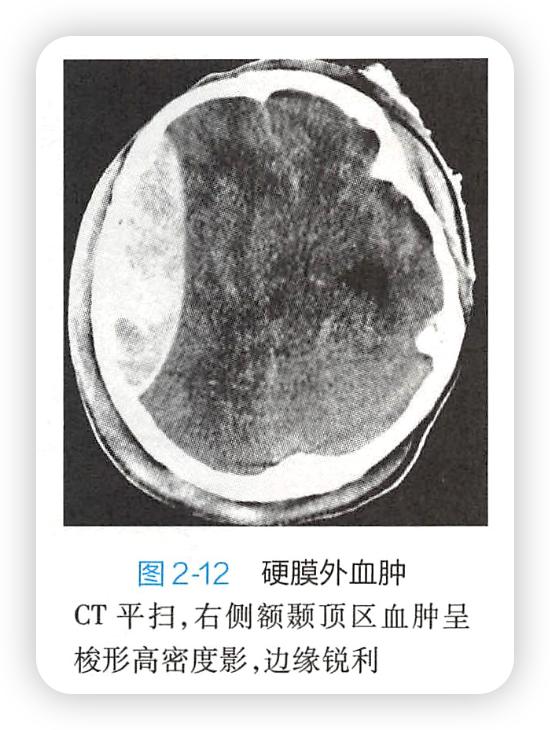
(1)平扫,颅板下方梭形/半圆形高密度灶,多在骨折附近,不跨越颅缝
硬膜下血肿:
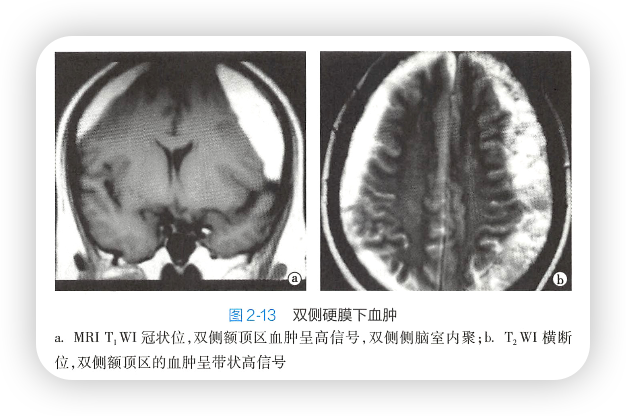
(1)平扫,急性期,颅板下新月形/半月形高密度影
(2)常伴有脑挫裂伤/脑内血肿
(3)脑水肿占位效应明显
(4)亚急性/慢性血肿,低/等/稍高/混杂密度灶
蛛网膜下腔出血:
(1)平扫,脑沟、脑池内密度增高影,形成铸型。
(2)大脑纵裂出血多见,中线区纵行窄带形高密度影。
(3)出血也见于:外侧裂池、鞍上池、环池、小脑上池
(4)一般7天左右吸收,CT阴性
五、原发性肝癌
1.临床
中老年,男性多见
85%为肝细胞癌(HCC),巨块型(≥5cm),结节型(5cm),弥漫型(1cm),小肝癌。
肝动脉供血,血供丰富。易侵犯门静脉、肝静脉,发生癌栓、肝内外血行转移,侵犯胆道引起梗阻性黄疸。肝门、腹膜后淋巴结转移。
2.影像
1)超声:初查
2)CT:确诊
直接征象:
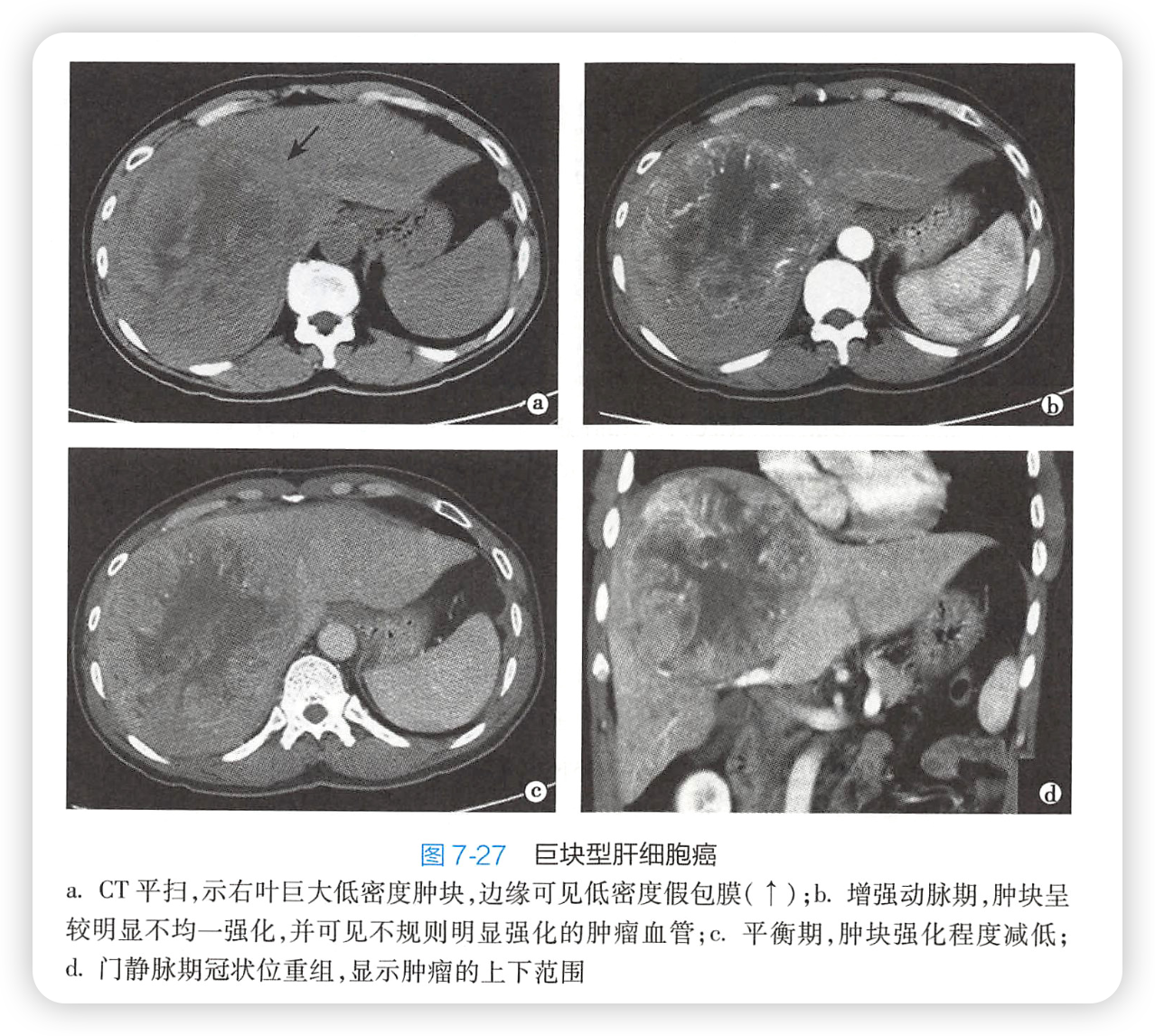
(1)巨块型:平扫,低密度肿块。中央坏死区更低密度。
(2)结节型:平扫,低密度肿块。
(3)弥漫型:平扫,境界不清的多发低密度小结节。
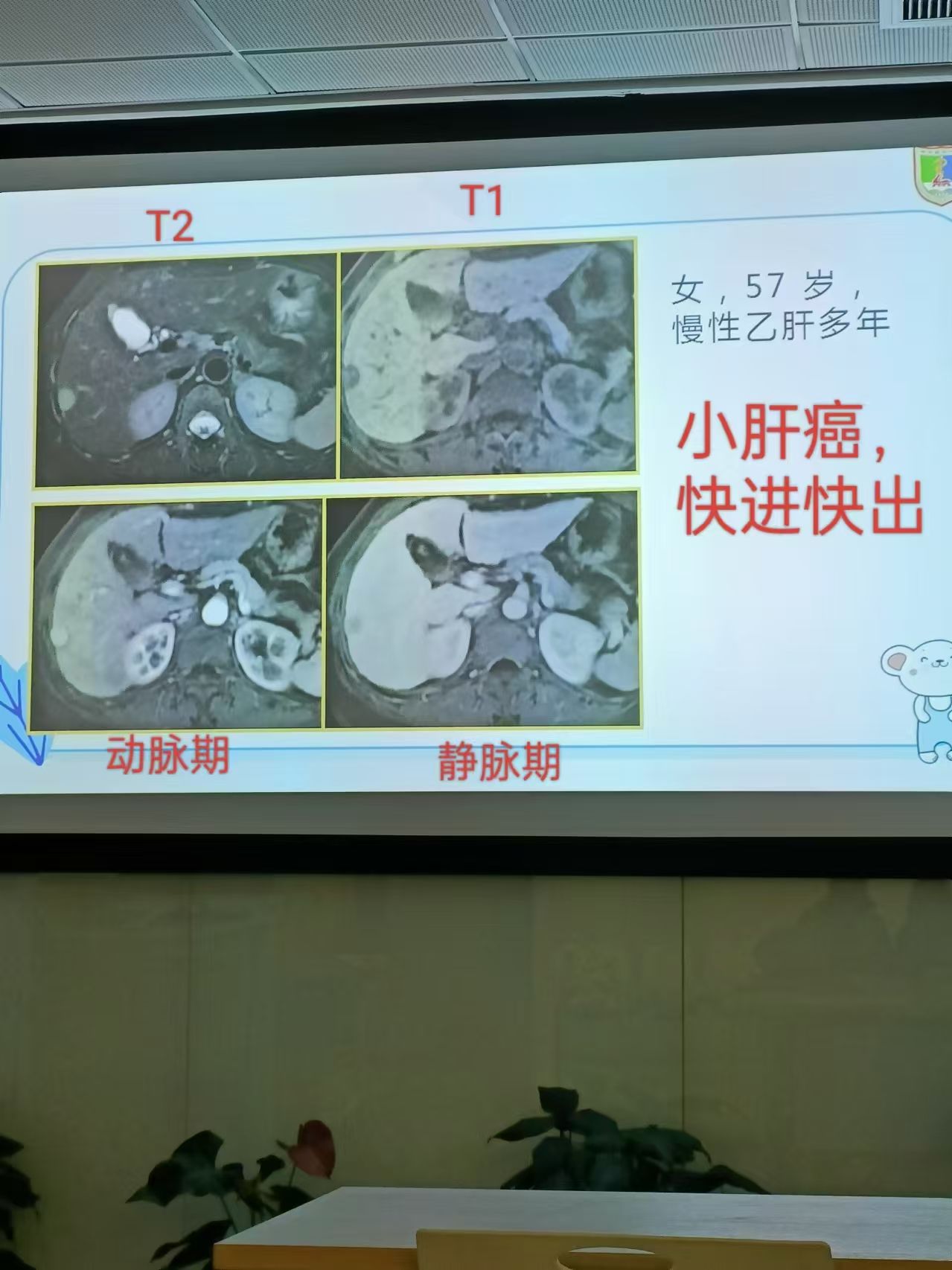
(4)增强扫描,整体呈“快进快出”,巨块型和结节型典型,
1. 动脉期:斑片状、结节状明显强化(因为肿瘤主要由肝动脉供血)。
2. 门静脉期:正常肝实质强化,密度明显升高,肿瘤相对低密度(因为缺乏门静脉供血)。
3. 平衡期:肿瘤密度持续减低,对比更明显。
(5)中央坏死液化区不强化。肿瘤假包膜一般在门静脉期/平衡期强化。弥漫型多数血供不丰富,强化不明显,但也可呈快进快出。
间接征象:
(1)静脉内癌栓:强化门静脉、腔静脉内低密度充盈缺损,门静脉期最清楚。
(2)淋巴结转移:常见肝门部、腹主动脉旁、腔静脉旁淋巴结增大
(3)胆管受侵犯:上方胆管扩张
(4)其他器官转移:肺、肾上腺、脾等转移灶
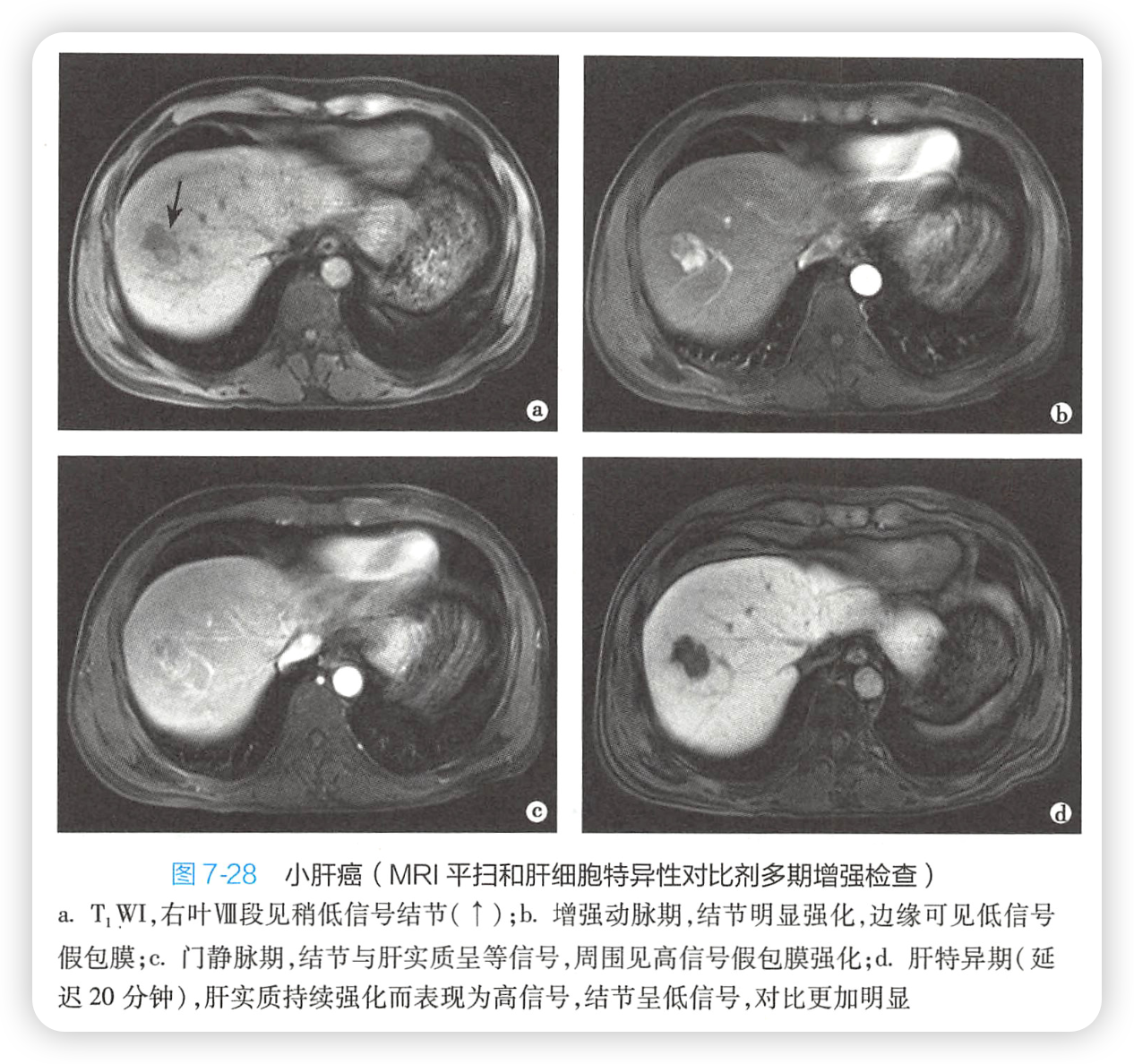
3)MRI:早期HCC
(1)T1WI低,T2WI稍高
(2)MRI肝细胞特异性对比剂增强扫描,动脉期、门静脉期同,肝特异期HCC细胞无法转运对比剂表现为低信号,敏感检出较小的HCC。
3.鉴别诊断
(1)肝腺瘤:多见于青年女性,口服避孕药,更易出血、脂肪变性,密度不均
(2)局灶性结节性增生:无快出,有延迟强化的中央瘢痕。MRI肝细胞特异性对比剂增强扫描为高密度。
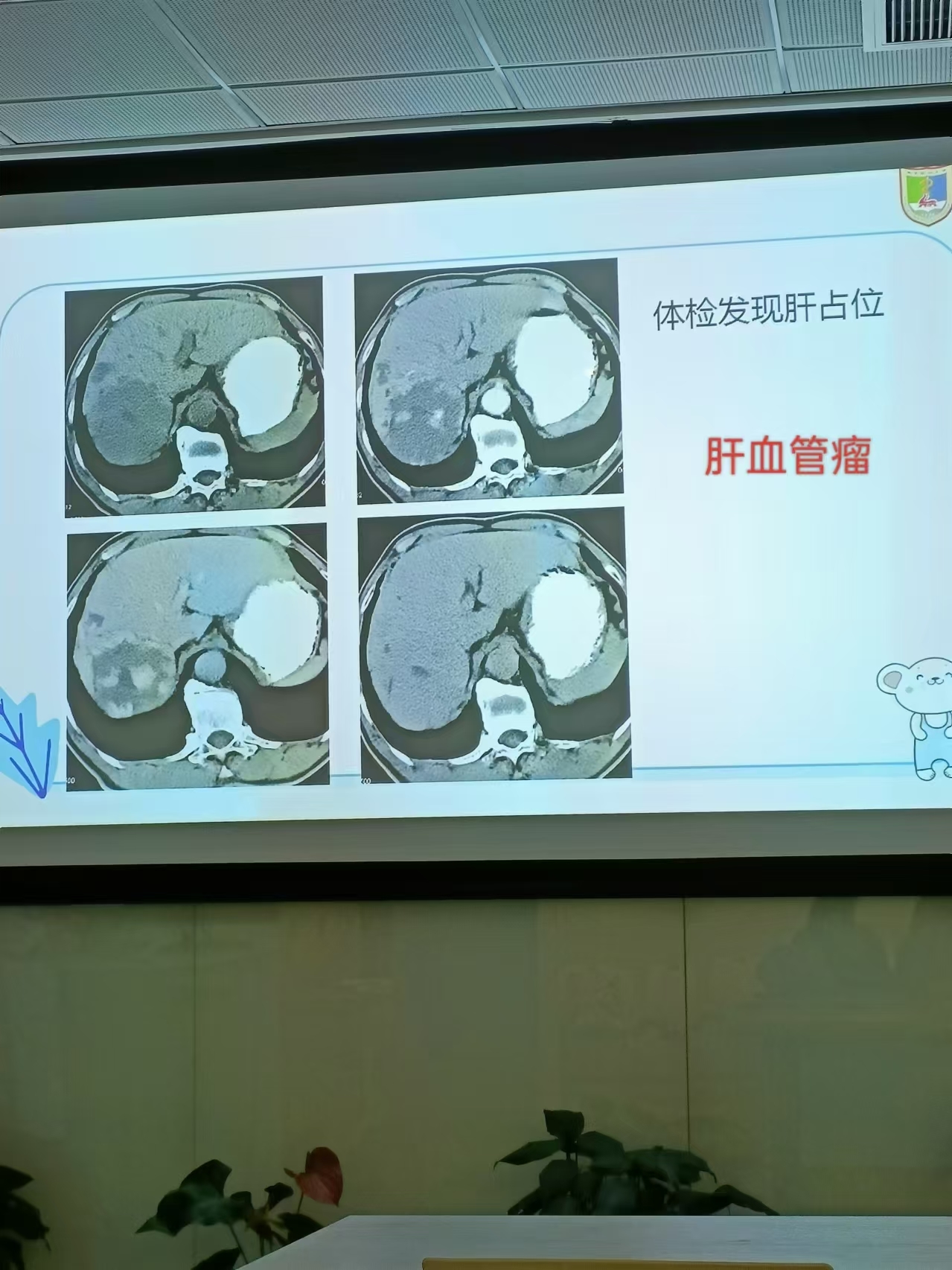
六、肝海绵状血管瘤
1.临床
中年女性
最常见肝脏肿瘤和肝脏最常见良性肿瘤。无包膜。偶有血栓,很少钙化。
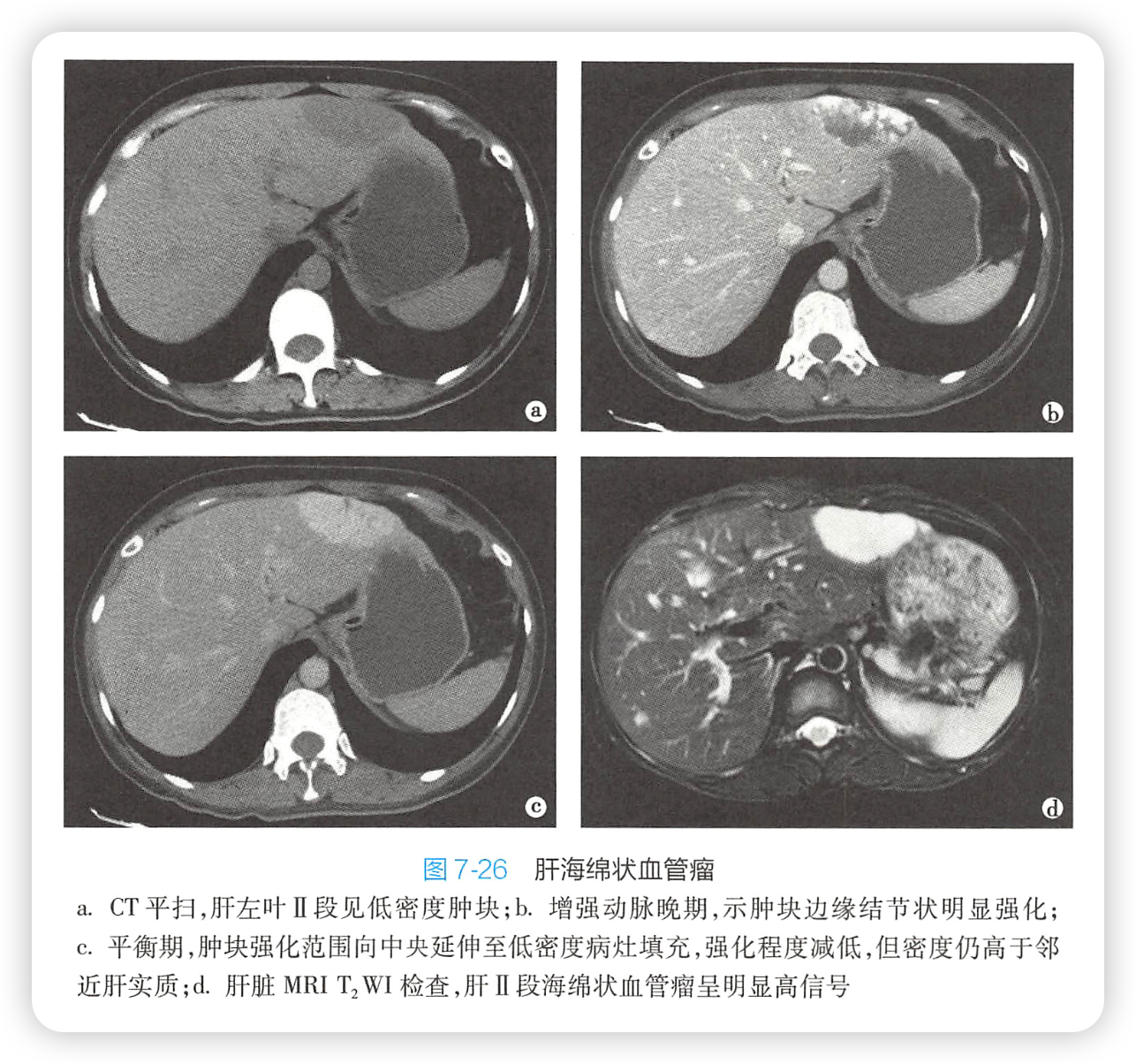
2.影像
1)超声:首选
2)CT:确诊
直接征象:
(1)边界清楚的低密度肿块。
(2)增强,整个过程向心性强化,早出晚归,快进慢出。
1. 动脉期:从周边部开始强化,多为结节状明显强化,程度类似同层主动脉。
2. 门静脉期:强化向肿瘤中心扩展。
3. 平衡期和延迟期:持续向中心扩展,强化程度减低,但仍高于或等于正常肝实质,最终全部肿瘤均一强化。
(3)即使延迟期,少数较大肿瘤中心仍有无强化低密度区,为纤维化或血栓。
间接征象:
CTA有时可见供血血管增粗,肿瘤压迫周围血管使之弧形移位。
3)MRI
T1WI均匀低,T2WI均匀高,灯泡征
七、胆石症与胆囊炎
【临床与病理】
胆结石依部位分为胆管结石和胆囊结石,统称为胆石症(cholelithiasis)。
胆石症为临床上常见病,以中年女性多见。
胆结石和慢性胆囊炎:
常见的症状为反复、突发性右上腹部绞痛,并放射至背部和右肩胛下区;
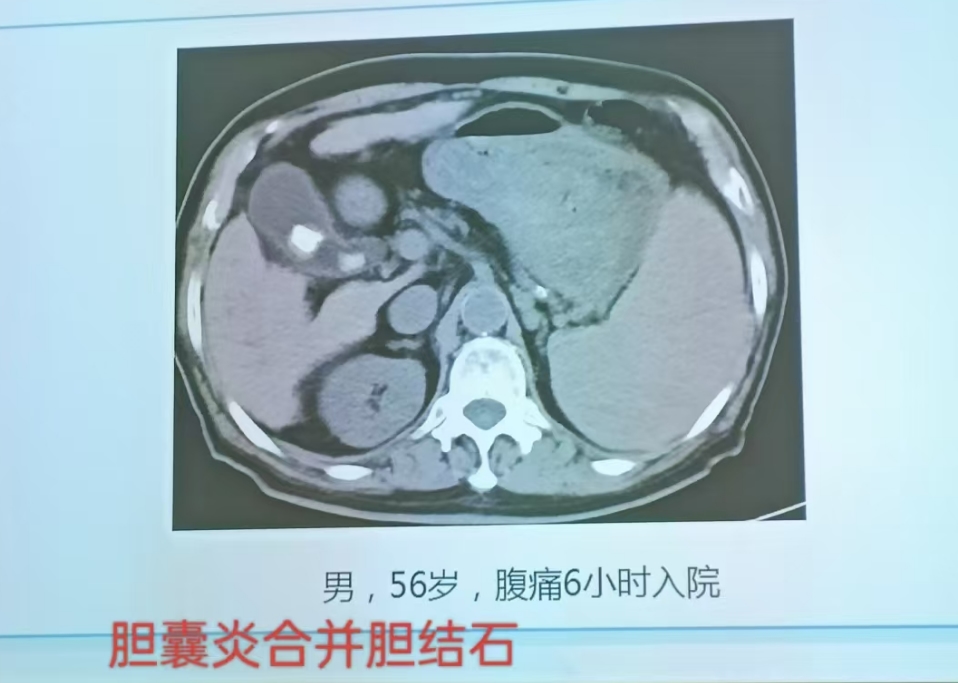
急性胆囊炎:
常表现持续性疼痛并阵发性绞痛,伴有畏寒、高烧、呕吐。检查右上腹压痛,墨菲(Murphy)征阳性。
【影像学表现】
X线:平片可显示的含钙量高的结石,称为阳性结石,而不能显示的含钙量低的结石,称为阴性结石。
胆囊阳性结石表现为右上腹大小不等、边缘高密度而中央低密度的环形、菱形、多角形致密影,聚集成堆时则呈石榴籽状,阴性结石平片不能显示。
胆管内结石,无论阳性或阴性结石,平片上均不易显示。ERCP可显示胆管内结石所致的充盈缺损。
超声:
- 胆系结石:典型表现为胆囊或胆管腔内一个或多个形态固定的强回声团、光斑或弧形强光带,后方伴有声影。发生在胆囊内者,强回声可随体位改变移动;泥沙型结石表现为胆囊后壁处细小的强回声光点带,后方伴较宽声影:结石填满胆囊时,胆囊无回声区消失,胆囊前半部呈弧形强光带,后方伴较宽声影,若伴有胆囊壁增厚,则出现“胆囊壁弱回声一结石强回声一声影”三联征。
- 胆囊炎:急性胆囊炎表现为胆囊增大:胆囊壁明显增厚,呈强回声,其间有弱回声带,重者呈多层弱回声带表现;慢性胆囊炎时胆囊可缩小;胆囊壁增厚、钙化,边缘毛糙,回声增强。
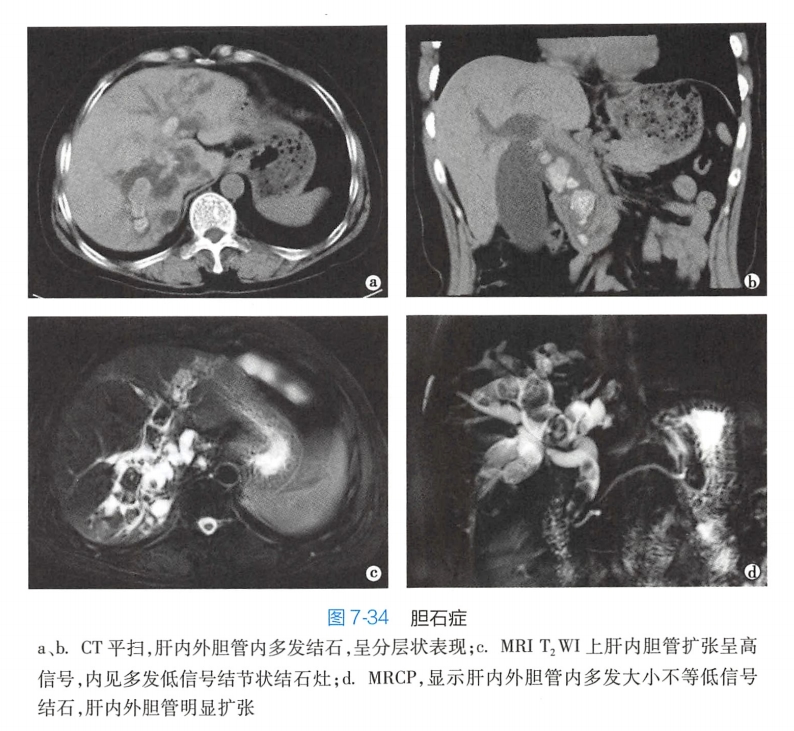
CT:
- 胆系结石:可见肝内、外胆管或胆囊内单发或多发、圆形、多边形或泥沙状的高密度影,密度均一、不均或分层(图7-34、b),阴性结石不能显示。
- 胆总管结石引起上部胆管扩张,在结石部位的层面,可见圆形高密度结石周围环有低密度胆汁,构成“靶征”,若部分围绕,则形成“新月征”。
- 胆囊炎:急性胆囊炎时,胆囊增大,直径>5cm,周围脂肪密度增高,胆囊壁弥漫性增厚超过3mm并呈分层状强化,其中周边无强化的环形低密度层,代表浆膜下水肿带或渗出;慢性胆囊炎则表现胆囊缩小,胆囊壁增厚,可有钙化,增强扫描呈均匀强化。
MRI:
- 胆系结石:基于结石成分不同,MRI上表现各异。通常,结石在T1WI上为低信号,部分为高信号或混杂信号;T2WI上均为低信号;MRCP可整体直观显示胆系内低信号结石的部位、大小、形态、数目等,但肝内胆管较小结石显示不佳;同时可显示胆管扩张及其程度(图7-34c、d)。
- 胆囊炎: T1WI和T2WI上显示胆囊增大和胆囊壁增厚;增厚的胆囊壁水肿层在T1WI为低信号,T2WI为高信号。
【诊断及鉴别诊断】
X线平片显示胆系结石有很大限度。
超声简便易行、可靠,为胆系结石的首选和主要检查方法。
CT对肝外胆管结石的显示要优于超声。
诊断困难的胆管阴性结石,可行MRI及MRCP检查,多可明确诊断。ERCP已不再用于检查胆系结石,而是用于介入治疗。
胆系结石超声、CT和MRI检查,征象明确,易于诊断。当结石合并胆囊增大或缩小,胆囊壁增厚并有分层或均一强化,则支持胆囊炎的诊断
八、急性胰腺炎
【临床与病理】
病因多为胆系疾病、酗酒、暴饮暴食等。
临床表现为突发性上腹部剧痛向腰背部放射,并有恶心、呕吐、发热等,重者可发生休克。本病多见于成年人,女性多见。
急性胰腺炎分为急性间质水肿性胰腺炎和坏死性胰腺炎2类,前者占80%~90%,表现为病变胰腺肿大变硬,间质充血水肿并炎性细胞浸润,胰周可伴有急性胰周积液(acute peripancreatic fluid collection,APFC),多数APFC能够自行吸收,如未吸收会演变成假性囊肿;
坏死性胰腺炎较少见,以广泛的胰腺坏死、出血为特征。胰液、炎性渗出、出血、坏死组织等聚积在胰腺内外,并可沿多条途径向腹膜后其他间隙或腹腔内扩展。急性坏死物(acute necrotic collection,ANC)发生在坏死性胰腺炎发病的一月内,可同时累及胰腺及胰周,并可延至盆腔,也可仅累及胰腺或胰周。
ANC与APFC的区别是前者含非液性成分,如实性成分或脂滴, ANC继续进展可形成成熟的壁,此时称为囊壁内坏死(walled-off necrosis,WON),其与假性囊肿的区别是囊内含有坏死组织或胰腺组织,不是单纯的液性成分。
尽管任何形式的病变都可以发生感染,但坏死物中的感染发生率高,此时影像学上病灶内可出现气体。
另外根据有无局部并发症及器官衰竭急性胰腺炎又分为轻、中、重度。多数患者病情较轻,如伴有坏死物感染、特别是器官衰竭,致死率会明显升高。
实验室检查,急性胰腺炎时,血和尿中淀粉酶明显增高。
【影像学表现】
超声:
- 急性间质水肿性胰腺炎:胰腺肿大,多为弥漫性,也可为局限性;边界常不清;内部回声稀少,回声强度减低;随病情好转上述改变可迅速消失。
- 坏死性胰腺炎:胰腺明显肿大;边缘模糊不清;回声强弱不均并伴有无回声或低回声区。急性胰腺炎常伴有邻近肠曲充气扩张,因而影响了超声的诊断效果。
CT:
- 急性IEP:
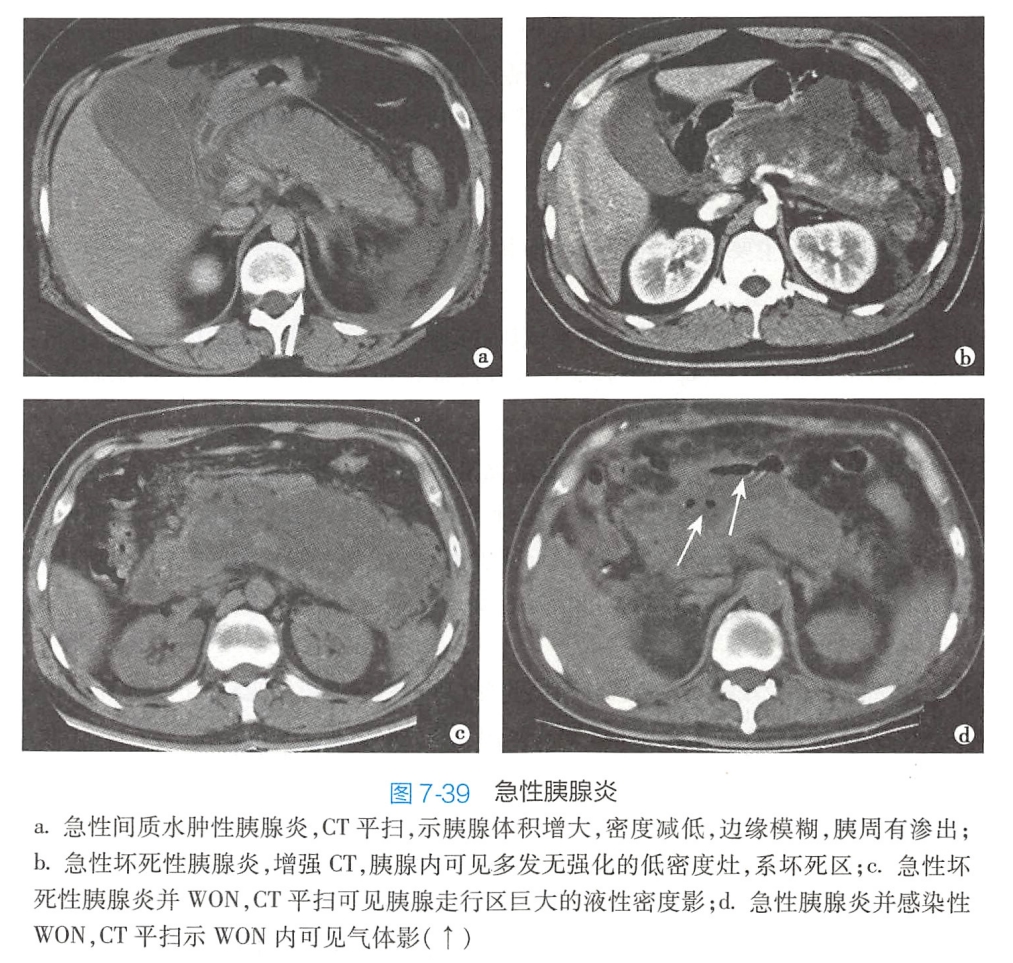
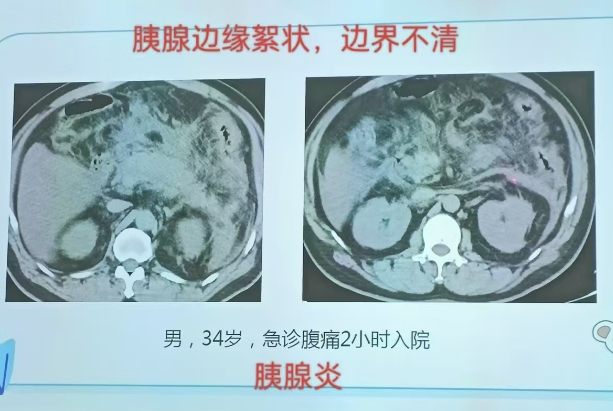
- 平扫检查,可见胰腺局限或弥漫性肿大(图7-39a),前缘多模糊不清,胰周脂肪常因炎性渗出而密度增高,左肾前筋膜增厚是常见表现
- 增强检查,胰腺均匀轻度强化,胰周渗出显示更加清楚。APFC表现为胰周无壁均匀的液性密度影:假性囊肿表现为局限性囊状低密度区,囊壁有强化,囊内没有坏死物。
- 坏死性胰腺炎:
- 平扫检查,除具有急性EP并更加显著外,还常见胰腺密度不均,坏死灶呈略低密度而出血呈高密度;
- 增强检查,胰腺强化不均,坏死灶无强化,据此可了解胰腺的坏死范围(图7-39),胰腺周围炎性渗出及坏死物可扩展至小网膜、脾周、胃周、肾前旁间隙、升、降结肠周围间隙、肠系膜以及盆腔,CT检查可显示相应部位的脂肪组织密度增高或呈水样密度。ANC的表现类似APFC,可见胰周和(或)胰腺内有液体聚集,同时伴有实性成分和脂滴等:WON表现为囊性包块内除有液性成分外,还有非液性成分,增厚的囊壁可出现明显强化,其内如出现气体,则提示为感染性WON(图7-39d)。
MRI:急性胰腺炎时:
- 平扫检查,可见胰腺肿大,边缘模糊不清;肿大的胰腺在T1WI上信号减低,T2WI上信号增高;出血灶在T1WI和T2WI上表现为信号不均匀或呈高信号;APFC见胰周液体在T1WI上呈低信号,T2WI上呈高信号;假性囊肿呈长T,、长T2信号,囊壁可见,囊内信号均匀,没有坏死物。ANC和WON的表现类似APFC和假性囊肿,但除液体信号外,还有非液体信号。
- 增强检查,表现同CT增强检查所见。由于MRI软组织分辨率高,能够很好地区分液性及非液性成分,因此诊断APFC、假性囊肿、ANC和WON的能力优于CT。
【诊断与鉴别诊断】
临床上,根据急性胰腺炎病史、体征及实验室检查结果,诊断并不困难。影像学检查的目的除进一步确诊外,主要是明确其类型、炎性渗出的范围及有无并发症,急性胰腺炎5~7天后局部并发症开始出现,坏死组织易于辨认,应做好必要的影像学复查。总之,CT和MRI对于了解病情的严重程度、决定治疗方案及预后评估均有重要意义,另外还有可能发现少数胰腺肿瘤性病变导致的急性胰腺炎。应当指出的是,在轻型急性E时,影像学检查可无明显阳性发现,此时诊断需依据临床资料而非影像学检查结果。
九、胰腺癌
1.临床
中老年,男女比为2。
通常指胰腺导管癌,占90%。易局部侵犯,胰周、肝门、腹膜后淋巴结转移(腹腔动脉周围最常见),65%在胰头。无痛性梗阻性黄疸。
2.影像:
1)超声
2)CT:
直接征象:
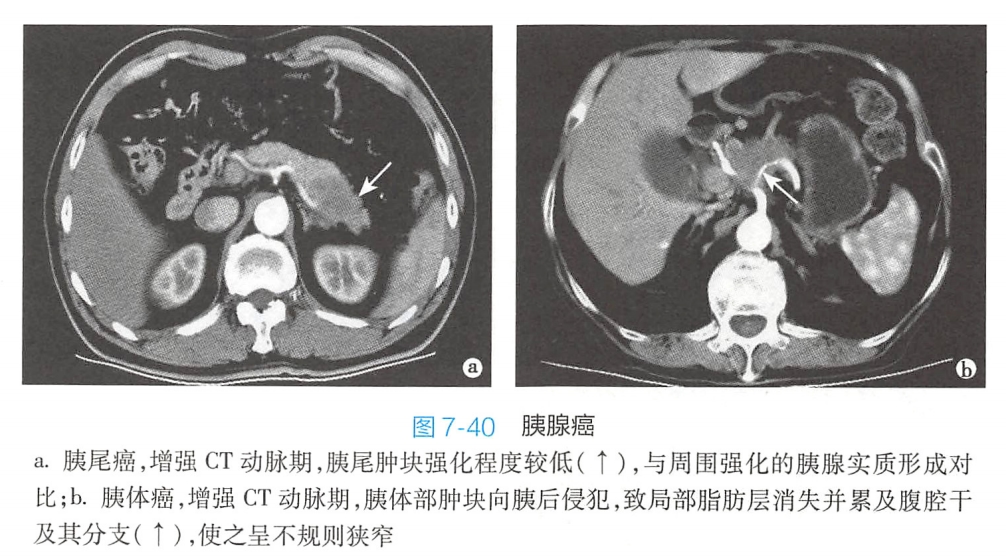
(1)平扫,与临近胰腺组织密度相似。较小者不易发现,较大者表现为胰腺局部增大,少数肿块内有坏死性低密度灶。
(2)增强,胰腺癌为乏血供肿瘤,强化不明显,相对低密度,一定程度延迟强化。
间接征象:
(3)肿块上游胰管常扩张
(4)胰头癌:“双管征”(胆总管和胰管扩张),可有胰腺体、尾部萎缩,潴留性囊肿,可并有急性胰腺炎的表现。
(5)向胰腺外侵犯,可致胰周低密度脂肪层消失
(6)胰周血管受累:增强,显示血管被包绕、狭窄甚至中断
(7)淋巴结转移:胰周、肝门、腹膜后多发软组织密度结节
(8)肝转移灶:低密度
3)MRI:
用于鉴别诊断
3.鉴别:
1)慢性胰腺炎合并胰头局限性增大:
(1)慢性胰腺炎:胰头纤维化改变,T2WI低信号。增强,持续渐进性。
胰头癌:动脉期低信号
(2)慢性胰腺炎:发现钙化、囊肿
(3)胰腺癌:侵犯或包埋血管
(4)胰腺癌:淋巴结转移
(5)慢性胰腺炎:胰管可扩张、狭窄,但少有截断
十、脾
脾(spleen)位于左上腹后外侧部,在左季肋区9~11肋的深面,属单核巨噬细胞系统器官,超声、 CT、MRI检查均易显示。
(一)检查技术
1.超声检查常作为脾疾病的首选影像检查技术。
2.CT检查能通过病变多期增强的强化表现提高脾疾病的诊断能力,同时可了解相邻组织器官,有助于对脾疾病进行全面评估。然而CT检查对脾疾病的定性诊断仍有一些限度。检查技术同肝脏CT检查。
3.MRI检查可作为CT检查后的补充方法,对某些脾疾病如脾脓肿、脾血管瘤和脾淋巴瘤的诊断常优于CT。检查技术同肝脏MRI检查。
(二)正常影像表现
1.超声检查
正常脾形态与切面方向有关,可呈半月形或类似三角形,外侧缘为弧形,内侧缘凹陷;脾门有脾动、静脉出入,为无回声平行管状结构:包膜呈光滑的细带状回声;脾实质呈均匀中等回声,略低于肝实质回声。CDFI显示脾静脉及其分支呈蓝色血流;脾门处脾动脉呈红色血流。脾厚径正常不超过4.5cm;脾长径正常范围为8~12cm;脾门处脾静脉内径小于0.8cm。
2.CT检查
正常脾前后径≤10cm、宽径≤6cm、上下径≤15cm;另一较简单的测量方法是在显示脾最大的横断层面上,正常脾外缘通常少于5个肋单位(肋单位为同层CT上肋骨和肋间隙的数目之和),但不及三维径线测量准确。平扫,脾形态近似于新月形或为内缘凹陷的半圆形,密度均匀并略低于肝脏;脾内侧缘常有切迹,其中可见大血管出入的脾门。
增强扫描,动脉期脾呈不均匀明显强化,静脉期和实质期脾的密度逐渐均匀。
3.MRI检查
脾在横断层上表现与CT类似,冠状位显示脾的大小、形态及其与邻近器官的关系要优于CT横断层。
(三)基本病变表现
1.脾数目、位置、大小和形态异常
脾数目增多如副脾和多脾,数目减少为脾缺如,位置异常如异位脾和游走脾,这些多为脾先天发育异常,变异脾的密度、信号强度及增强检查表现均与脾相同。脾增大在影像上表现为脾各径线超过正常值范围,明显超出者易于辨认,不明显者由于个体间有较大差异而难以判别。超声、CT和MRI均易发现脾形态异常,如占位性病变突出脾表面时可致脾边缘与轮廓改变,脾破裂可见脾轮廓不规整、形态失常。
2.脾密度和信号异常
脾内钙化灶在CT上表现为极高密度影,MRI上呈低信号影;
脾梗死灶多呈楔形,CT上密度减低,MRI上呈T1WI低信号,T2WI高信号影,无强化;
脾外伤新鲜出血在CT上表现为高密度影,MRI上表现为高低混杂信号影,出血的密度、信号变化与损伤的时间有关;
脾囊肿在超声、CT和MRI上与其他部位囊肿表现相同;
原发和转移性脾肿瘤在CT上多呈稍低密度影,MRI上常呈T1WI低信号,T2WI高信号影;
CT、MRI增强检查可提高病灶检出率,但由于脾肿瘤影像表现多类似,定性诊断时有困难。
(四)疾病诊断
1.脾肿瘤
【临床与病理】脾肿瘤(splenic tumor)较少见,良性肿瘤常见的有血管瘤、错构瘤及淋巴管瘤,其中成人以海绵状血管瘤多见,可单或多发,肿瘤生长缓慢,临床多无症状。恶性肿瘤分为原发恶性肿瘤、转移性肿瘤和淋巴瘤。其中以淋巴瘤多见,可以是全身性淋巴瘤累及脾,也可以原发于脾,前者多见;大体病理上脾可仅显示为弥漫性肿大,也可表现为弥漫的细小结节、多发肿块或单发大肿块。临床上脾淋巴瘤多见于40岁以上,可有长期发热、浅表淋巴结肿大、脾大、左上腹疼痛等症状。
【影像学表现】
(1)海绵状血管瘤
超声:①二维超声检查,肿瘤多表现为圆形界清高回声,内部回声均匀或呈蜂窝状表现;②CDI示瘤内无血流,周围有点状或短线状血流。
CT:①平扫,多表现为圆形、类圆形低密度病变,边界清楚,可有囊性成分和钙化,大的病灶中央因有瘢痕形成,显示为更低密度区;②增强扫描,早期从边缘开始强化,一般不表现为肝血管瘤时典型的结节状强化,但出现渐进性向中央填充,最后大多能完全或大部充填,密度等于或高于脾脏,与肝血管瘤表现类似(图7-43);有的肿瘤早期强化不明显,延迟后趋向等密度;也有的肿瘤表现为强化不均匀,即使在延迟期仍呈斑驳状强化表现。
MR:①平扫检查,由于瘤内有扩张的血窦,血流缓慢,故肿块在TWI多为界限清楚的低信号, T,WI呈高或明显的高信号影:②增强检查,表现类似CT增强检查。
(2)淋巴瘤超声:
表现与其病理类型相关:①脾弥漫性肿大,脾实质回声诚低或正常,一般光点分布较均匀;②脾内结节和肿块,显示为脾实质内单发或多发散在、界限清楚的圆形低回声结节或肿块,其内部回声均或不均,多个病灶可相互融合而呈分叶状团块,病灶之间隔以线状高回声带。 CT:可仅显示脾增大,也可显示脾内局灶性病变伴或不伴脾增大。脾内局灶性病变表现为:①平扫,可见脾内单发或多发稍低密度灶,边界清或不清:②增强扫描,肿块呈轻度不均匀或斑片状强化,与正常强化脾实质分界清楚。在全身淋巴瘤累及脾时,在显示脾异常表现的同时,还可发现邻近淋巴结增大和全身淋巴瘤表现(图7-44)。
MR:①平扫检查,可仅表现为脾弥漫性增大,也可发现脾内单个或多个大小不等的长T,长T2或混杂信号圆形结节或肿块,边界清或不清:②增强检查,脾内肿块呈轻度强化,信号较正常脾为低,典型者呈“地图样”分布,可伴有脾周或其他部位淋巴结增大。【诊断与鉴别诊断】典型的海绵状血管瘤影像诊断并不困难,不典型者需与其他脾脏富血供肿瘤和病变鉴别。脾淋巴瘤超声、CT和MRI检查时,可有不同表现:①仅表现脾增大的脾原发淋巴瘤,诊断困难,需与其他病因所致的脾增大鉴别:②仅表现为脾内单发或多发病灶的脾原发淋巴瘤,需与转移瘤等鉴别:③同时并有脾内病灶和邻近或其他部位淋巴结增大表现时,多提示为全身淋巴瘤累及了脾,但仍需与广泛的转移瘤鉴别。对于脾淋巴瘤,影像学检查的价值在于:①已明确淋巴瘤患者,发现脾淋巴瘤,有助于临床分期和治疗;②未确诊患者,显示脾异常需进一步评估,行PET检查常有助诊断:③可用于评估脾淋巴瘤治疗后效果。
2.脾脓肿
【临床与病理】脾脓肿(splenic abscess)少见,是细菌侵入脾内形成的局限性化脓性感染;多继发于全身性感染的血源性播散或脾周感染的蔓延,也可为外伤、梗死后的并发症。脓肿为单房或多房,可孤立或多发。临床上,表现为全身感染症状并脾区疼痛。
【影像学表现】 X线:平片可见左膈升高,常伴有胸腔积液,表现无特征。超声:二维超声①初期,可无异常或显示稍低回声区:②脓肿形成期,呈不规则或圆形无回声区,其内可见散在光点回声,若有气体,则出现强回声气体样反射:周边有高回声带环绕:CDFI和频谱多普勒见脓肿壁有较丰富的血流信号,为动脉血流。动态观察,无回声区可进行性增大,抗感染治疗后,无回声区范围可明显缩小。 CT:①平扫检查,典型脓肿表现为脾内圆形或椭圆形界清低密度区,单发或多发,CT值差别较大,一般<30HU,有时脓肿内有气体影:②增强检查,脓肿壁呈环状强化,脓肿中心不强化。 MR:①平扫检查,脾脓肿的脓腔表现为圆形T,WI低信号和T2WI高信号;病灶周围可见水肿,呈 T,WI低信号和T,WI高信号:②增强检查,表现同CT增强检查。
【诊断与鉴别诊断】根据影像学表现,结合临床,一般可做出诊断。CT对气体、液体的检出敏感,对本病诊断和鉴别诊断有重要意义。脾脓肿应与膈下脓肿、脾囊肿等鉴别,诊断困难时可行超声或CT引导下穿刺活检。
3.脾梗死
【临床与病理】脾梗死(splenic infarction)为脾动脉或其分支栓塞所造成的局部脾组织缺血坏死。病因包括:动脉粥样硬化、血栓形成、慢性白血病所致脾动脉内皮细胞下白细胞浸润、镰状细胞性贫血所致微循环等,可单发,也可数个病灶同时存在或融合:病灶多呈楔形,底部位于被膜面,尖端指向脾门。脾梗死可无症状或有左上腹疼痛、左侧胸腔积液、发热等表现。
【影像学表现】
超声:①二维超声:脾实质内有单发或多发楔形或不规则形低回声区,底部朝向脾外侧缘,尖端指向脾门;内部有高回声光点或呈蜂窝状回声:②CDFI检查,显示病变区内无血流信号。梗死灶坏死液化后可形成假囊肿,出现液性无回声区;陈旧性梗死灶纤维化、钙化时,回声明显增强,后方可伴有声影。
CT:
- 平扫检查,典型表现为尖端朝向脾门、边界清楚的楔形低密度区:
- 增强检查,低密度区无强化,与周围正常强化脾实质对比更加清楚(图7-45)。
MR:
- 平扫检查,梗死区信号依梗死时间而不同,急性和亚急性梗死区在T1WI和T2WI上分别为低信号和高信号影;而慢性期由于梗死区有瘢痕组织和钙化形成,在MRI各种序列上均呈较低信号改变。
- 增强扫描,病灶无强化。
【诊断与鉴别诊断】在脾梗死,影像学上出现病灶呈楔形这一典型表现时,诊断不难;若形态不规则,则需与脾脓肿脾破裂出血等鉴别。超声CDFI检查无血流,CT和MRI增强检查病灶无强化是脾梗死的特征表现,也是鉴别诊断的主要依据。
十一、急性阑尾炎
1.临床
定位不清脐周疼痛,伴恶心、呕吐、发热及食欲缺乏等。6-8/10+h后逐渐下移固定右下腹部(转移性右下腹痛,特征)。查体麦氏点压痛、反跳痛。实验室白细胞和中性粒细胞升高。
2.影像
(1)超声:阑尾和粪石,后者伴声影;阑尾管径>6mm,呈不可压闭的、一侧盲端管状结构。
(2)CT:阑尾扩张,管径>6mm,壁增厚,增强强化。阑尾周围炎,周围(脂肪)“条纹征”即周脂肪内斑点/条纹状模糊英、局部筋膜增厚、系膜密度增高等。阑尾粪石,其他有盲肠增厚、阑尾周液体积聚、“箭头征”(肠道内造影剂汇集在盲肠尖端(阑尾起始部)形成箭头样或鸟嘴样改变)。
十二、脑出血
属于出血性脑血管疾病,多发于中老年高血压和动脉硬化患者。
【临床与病理】
自发性脑内出血多继发于高血压、动脉瘤、血管畸形、血液病和脑肿瘤等,
血管畸形性脑出血在年轻人中多见,高血压性脑出血以老年人常见。
在后者,出血好发于基底节、丘脑、脑桥和小脑,易破入脑室;血肿及伴发的脑水肿引起脑组织受压、坏死和软化。
临床上根据出血时间及血肿病理演变过程将脑出血分为
- 超急性期 (12小时以内 )、
- 急性期 (12小时至2天)、
- 亚急性期 始于出血后 2 ~ 7 天
- 慢性期
各期时间长短与血肿大小及患者年龄有关。
【影像学表现】
CT平扫:
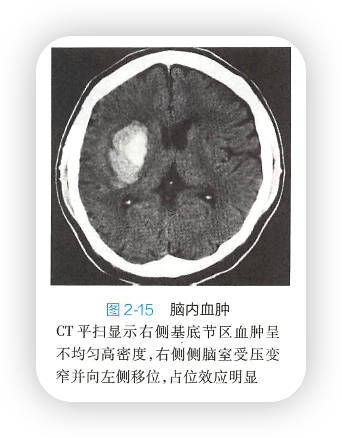
- 急性期:血肿呈边界清楚的肾形、类圆形或不规则形均匀高密度影;周围水肿带宽窄不一,局部脑室受压移位(图 2 - 1 5 );破 入 脑 室 可 见 脑 室 内 高 密 度 积 血 ;
- 亚 急 性 期:始于出血后2 ~ 7 天 ,可 见 血 肿 缩 小 并 密 度 减 低 ,血 肿 周 边 变模 糊 ;水 肿带增宽;小血肿可完全吸收;
- 慢性期,为出血2 个月以后,较 大血肿吸收后常遗留大小不等的裂隙状囊腔;伴有不同程度的脑 萎缩。
CT增强扫描:血肿早期多不强化,亚急性期由于血肿周围炎症反应及新生毛细血管而出现环状强化。
MRl:普通检查,脑内血肿的信号随血肿期龄而变化:等等高低,高低 低高 高
- 超急性期:血肿T1WI 呈等信号,T2WI呈稍高信号;
- 急性期:血肿T1WI 呈等信号,T2WI 呈稍低信号;
- 亚急性期:亚急性早期,血肿T1WI 信号由周边到中心逐渐 增 高 ,T2W I 呈 低 信 号 ;亚 急 性 晚 期 T 1W I 及 T2WI 均高信 号 ;
- 慢 性 期 :囊 肿 完 全 形 成 时 T1W I 呈 低信号,T2WI呈高信号;由于周边含铁血黄素沉积T2WI 上可见低信号环,此期MRI显示比CT敏感。
超急性期和急性期血肿显示均不如 CT清楚。
【诊 断 与 鉴 别诊 断】
根据典型的CT、MRI 表现和突发的临床症状,脑内出血容易诊断 。CT和MRI 对脑出血的检查有很强的互补作用,为脑出血不同时期的鉴别诊断提供了有力帮助。临床症状不明显的脑出血在吸收期CT检查时可能为等密度,需和脑肿瘤鉴别。
十三、脑梗死
缺血性脑血管疾病,其发病率在脑血管疾病中居首位。
【临床与病理】
脑梗死为脑血管闭塞所致脑组织峡血性坏死。
病理上分为缺血性、出血性和腔隙性脑梗死。
【影像学表现】
(1 )缺血性梗死
CT:
- 平扫,在发病24小时内常难以显示病灶;24 小时后表现为低密度灶,部位和范围与闭塞血管供血区一致,皮髓质同时受累,多扇形;可有占位效应,但相对较轻;
- 增强扫描,发病当天,灌注成像即能发现异常,表现病变区脑血流量明显减低;其后普通增强可见脑回状强化。1~2 个月后形成边界清楚的低密度囊腔,且不再发生强化。
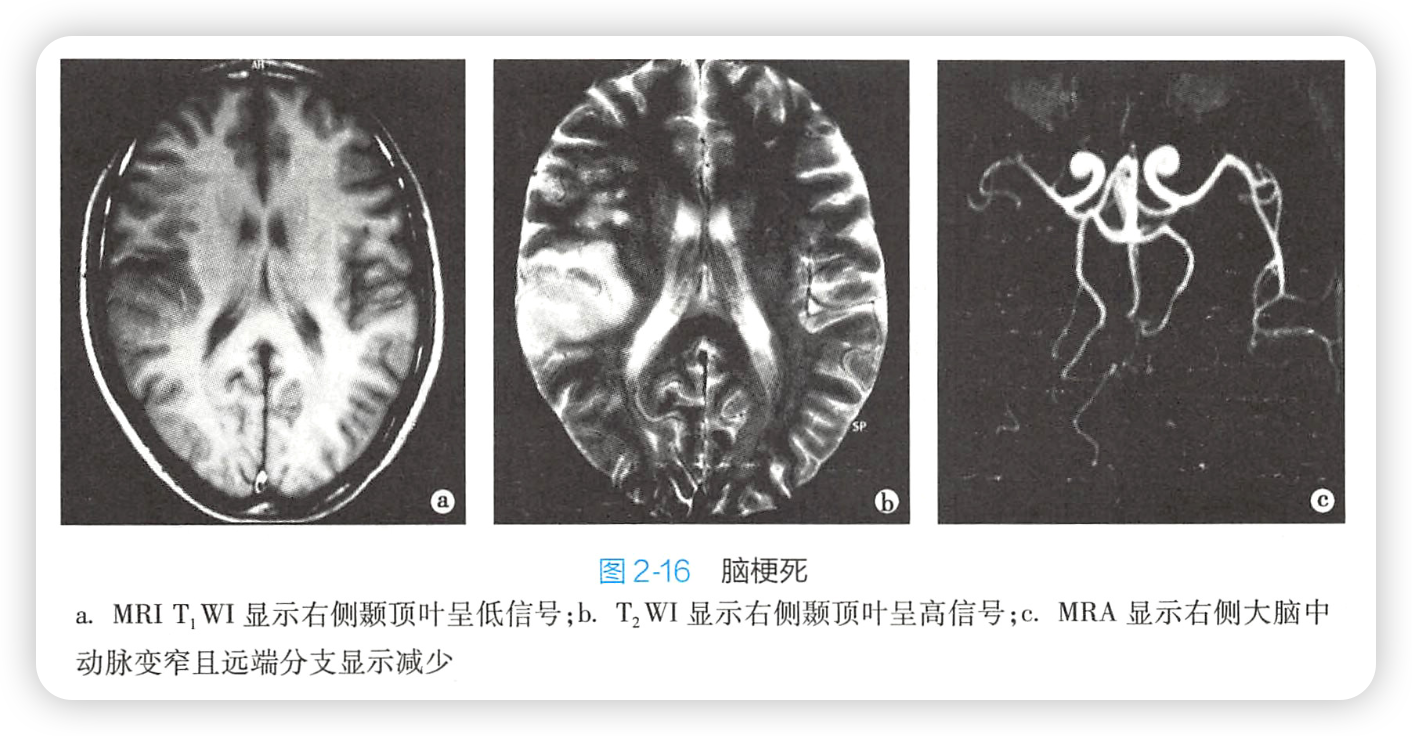
MRI:对脑梗死灶发现早 、敏感性高: - 发病后1 小时即可见局部脑回肿胀 ,脑沟变窄 ,随之出现T1WI低信号、T2WI高信号影 (图 2 - 1 6 a 、b );
- DWI 检 查 可 更 早 地 检 出 脑 缺 血 灶 ,表 现 为 高 信 号 ;
- M R A 检 查 还 能 显 示 脑 动 脉 较 大 分 支 的 闭 塞 (图 2 - 1 6 c )。
(2)出血性梗死
常发生在缺血性梗死一周后。
CT:平扫,呈低密度脑梗死灶内,出现不规则斑点、片状高密度出血灶,占位效应较明显。
MRI:普通检查,梗死区内出现T1WI 高信号灶。
(3) 腔隙性梗死
系 深 部 髓 质 穿 支 动 脉 闭 塞 所 致 。 缺 血 灶 为 1 0 ~ 1 5 m m 大 小 , 好发于基底节、丘脑、小脑和脑干,中老年人常见。
CT:平扫,发病24小时后,可见脑深部的片状低密度区,无占位效应。
MRl :早期DWI 检查即可发现腔隙性梗死灶,表现为小的高信号区;其后呈T 1WI 低信号、T2WI 高信号表现;
DTl 重建可显示皮质脊髓束破坏情况(图2-17)。
【诊断与鉴别诊断】
根据上述典型脑梗死的CT和MRI 表现,结合病史多可明确诊断。
表现不典型时应注意与星形细胞肿瘤、病毒性脑炎等相鉴别:星形细胞肿瘤占位表现常较脑梗死更显著,且多呈不规则强化;病毒性脑炎常有发热,病灶可为双侧对称性,且脑脊液特异性抗体检查为阳性。