单糖
从结构上,单糖可分为醛糖(aldose)和酮糖(ketose)。根据分子中所含碳原子数目又可分为三碳(丙)、四碳(丁)、五碳(戊)和六碳(己)糖。
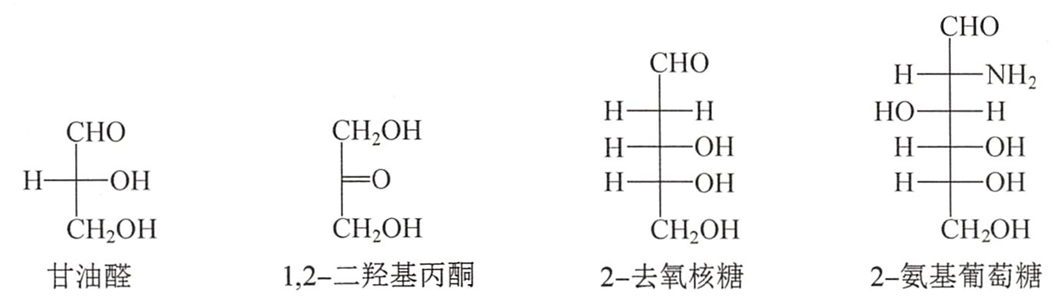
最简单的醛糖是甘油醛(glyceraldehyde),最简单的酮糖是1,3-二羟基丙酮。
自然界最广泛存在的葡萄糖是己醛糖。
果糖为己酮糖,在蜂蜜中含量最高。在生物体内戊糖和己糖最为常见。
有些糖的羟基可被氢原子或氨基取代,它们分别被称为去氧糖和氨基糖。例如2-去氧核糖,2-氨基葡萄糖。
一、构型和开链结构
单糖的立体化学结构可用R、S构型标记法,但目前人们仍习惯用D/L构型标记法。人们习惯用Fisher投影式表示单糖的结构,竖线表示碳链,羰基具有最小编号;将编号最大的手性碳(即离羰基最远的一个手性碳)的构型与D-甘油醛相比较,构型相同的为D-构型糖,反之为L-构型糖。例如:
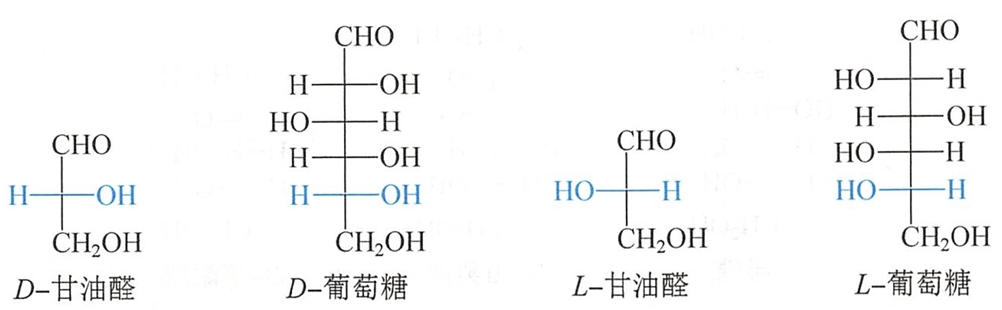
对于其他单糖的构型也都是以甘油醛作为标准而定的。
绝大多数单糖具有旋光性,含三个手性碳的戊醛糖应有8个对映异物体,含4个手性碳的己醛糖有16个对映异构体。
酮糖比相应的醛糖少一个手性碳原子,因此酮糖异构体数目也相应减少,如己酮糖有8个对映异构体。
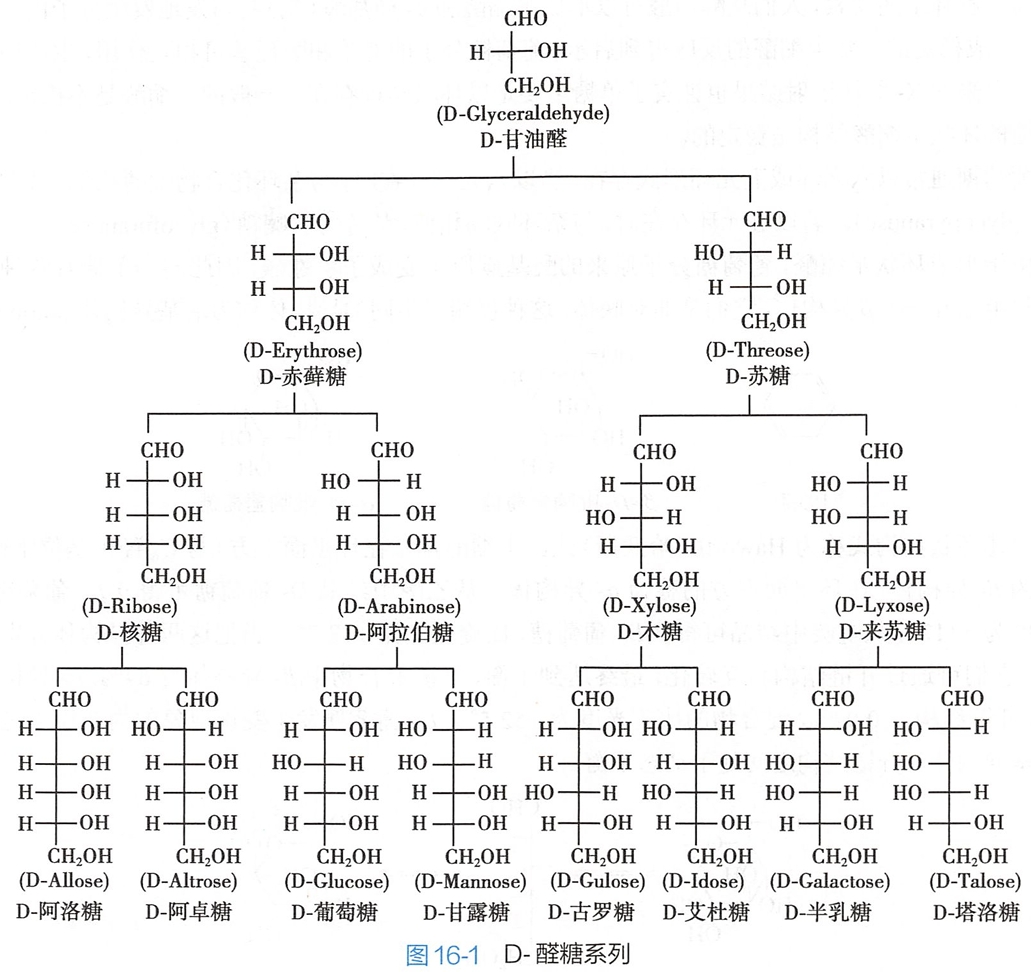
单糖的名称常根据其来源采用俗名。图16-1列出含有3C~6C的各种D-醛糖,它们多数存在于自然界,如D-葡萄糖广泛存在于生物细胞和体液里;半乳糖存在于乳汁中;D-核糖为核酸的组成部分,广泛存在于细胞中;少数D-醛糖是人工合成的。
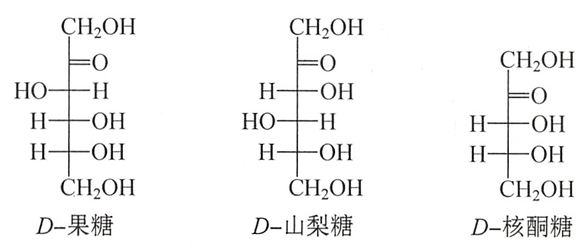
在自然界中也发现一些D-酮糖。它们的结构一般在C2位上具有酮羰基。例如:D-果糖、D-山梨糖和D-核酮糖等。
二、变旋光现象和环状结构
尽管单糖的开链结构表明单糖分子中含有羰基,但人们发现某些与这种开链结构实验事实不相符:
- 一般醛在干燥HCl存在下与两分子甲醇反应生成缩醛,但葡萄糖只与一分子甲醇反应生成稳定化合物;
- D-葡萄糖在不同条件下可得两种结晶,从冷乙醇中可得熔点为146℃,比旋光度为+112°的晶体,而从热吡啶中可得熔点为150℃,比旋光度为+18.7°的结晶;
- 上述两种晶体的糖溶于水后比旋光度都会发生变化并都在+52.5°时保持恒定不变,这种比旋光度发生变化的现象称为变旋光现象(mutarotation);
- 固体葡萄糖在红外光谱中不显示羰基的伸缩振动峰。
为了解释上述观察,人们从醇与醛可以形成半缩醛和δ-羟基醛(酮)易自发地发生分子内的亲核加成,生成稳定的环状半缩醛的反应得到启示,葡萄糖分子的醛基和醇羟基可相互作用,生成环状半缩醛。
后来的X-射线衍射结果也证实了单糖主要是以环状结构存在。一般的半缩醛是不稳定的,但葡萄糖的环状半缩醛结构是稳定的。葡萄糖通常以六元环或五元环形式存在,当以六元环存在时,与杂环化合物吡喃相似,故称为吡喃糖(glycopyranose)。若以五元环存在时,与杂环呋喃相似,故称为呋喃糖(glycofuranose)。
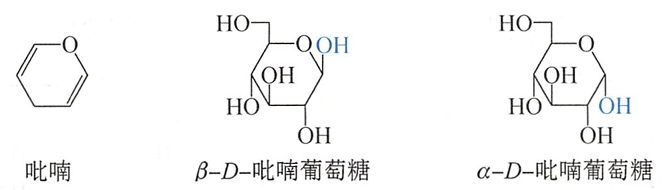
由于形成环状半缩醛,葡萄糖分子原来的醛基碳原子变成了手性碳,因此同一单糖有两种不同的环状半缩醛一α、β异构体,它们是非对映体,这种仅端基不同的异构体称为端基异构体(anomer)。
上述环状结构式称为Haworth(哈武斯)式。半缩醛羟基在环平面上方(与C6羟甲基位于同侧)的称为β-异构体,在环平面下方的称为α-异构体。
从乙醇中结晶D-葡萄糖可得α-D-葡萄糖,比旋光度为+112°,从吡啶中结晶可得β-D-葡萄糖,比旋光度为+18.7°。当把这两种异构体分别溶于水中,它们可通过开链结构相互转化,最终达到平衡,平衡混合物中β-异构体占64%,α-异构体占 36%,开链结构占0.02%,混合物的比旋光度为+52.5°。
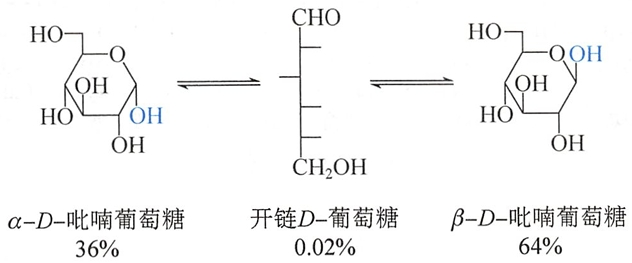
D-葡萄糖发生变旋现象的内在原因是这两种端基异构体与开链结构之间处于动态平衡。
由于开链结构含量极低,因此仅存在于开链结构中的羰基的特征吸收在葡萄糖的光谱中不显著。
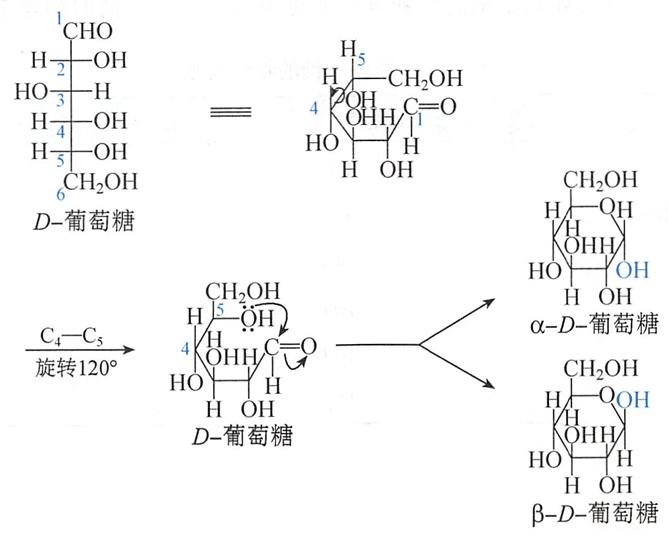
我们以D-葡萄糖为例说明如何从己醛糖直链的Fischer投影式改变成Haworth式。为了使C5羟基靠近醛基,可使C4一C5间的单键旋转120°,此过程没有任何键断裂,因此C5构型没有改变,但产生了有利于成环的取向,使C5羟基有利于向C1羰基进攻,最后C5羟基分别从羰基平面两侧进攻羰基碳,得到两个端基异构体一α-D-吡喃葡萄糖和β-D-吡喃葡萄糖。
从上述Fischer投影式转变为Haworth式可以看出在Fischer式中处于右侧的羟基(指连在手性碳上的羟基)应在Haworth式环平面的下边,左边的羟基在环平面的上边。D-构型的端基一CH2OH也在Haworth式环平面上边。
许多单糖都具有环状结构,例如:β-D-呋喃果糖和β-D-呋喃核糖。
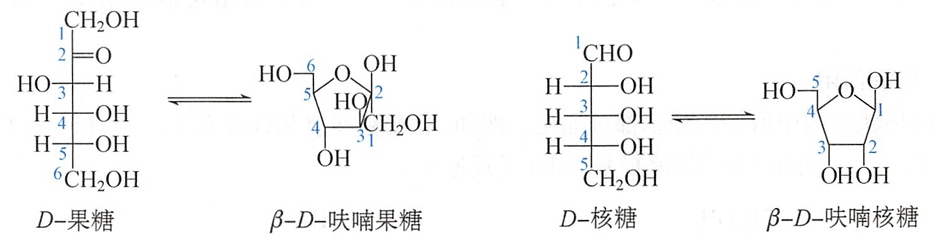
α-D-吡喃葡萄糖和β-D-吡喃葡萄糖简称为α-D-葡萄糖和β-D-葡萄糖。在D-葡萄糖水溶液中, β-D-葡萄糖的含量比α-D-葡萄糖高(64:36)。Haworth式把环当作平面,不能准确表示D-葡萄糖的立体结构,也就不能解释为什么在水溶液中β-D-葡萄糖含量比α-D-葡萄糖高。更符合吡喃糖实际结构的是其构象式。下面是D-葡萄糖的两种椅式构象式。
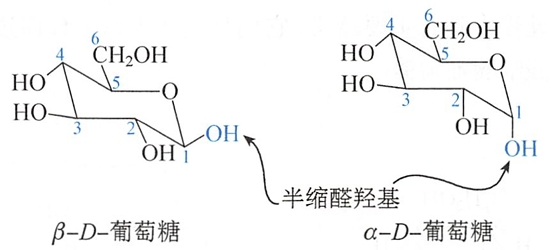
β-D-葡萄糖分子的取代基(含半缩醛羟基)全部为e键;α-D-葡萄糖与β-D-葡萄糖不同的是其半缩醛羟基OH处于α键。显然β-D-葡萄糖比α-D-葡萄糖更稳定,因此D-葡萄糖在水溶液的动态平衡中,β-异构体的含量要高于α-异构体。
书写吡喃糖(如D-葡萄糖、D-半乳糖等)的构象式时,含“O”的六元环要写成像上述D-葡萄糖的形式,因为此种含“O”的六元环相对稳定。 (氧的意思)
三、物理性质
单糖都是无色结晶体,有吸湿性,极易溶于水,难溶于酒精,不溶于醚。单糖易形成过饱和溶液糖浆。水-醇混合溶剂常用于糖的重结晶。单糖有甜味,不同的单糖甜度不同,果糖最甜。除二羟基丙酮外单糖都有旋光性,具有环状结构的单糖具有变旋现象。
四、化学性质
单糖分子中既含有羰基又含有多个羟基,故具有一般醛酮和醇的性质,如醛酮的羰基可发生还原反应,醇羟基可发生酯化反应。又由于这些官能团处于同一分子内相互影响,所以又具有一些特殊性质。
(一)成酯作用
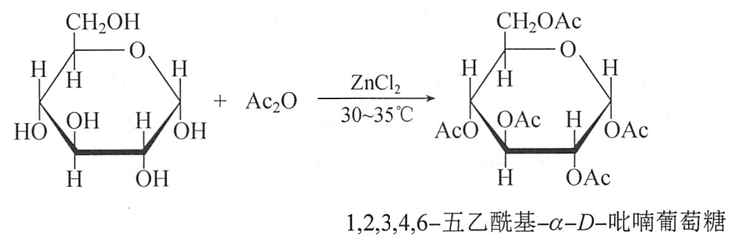
单糖的环状结构中所有的羟基都可酯化。例如,葡萄糖在氯化锌存在下,与乙酐(Ac2O)作用生成五乙酸酯。五乙酸酯已无半缩醛羟基,因此无还原性。
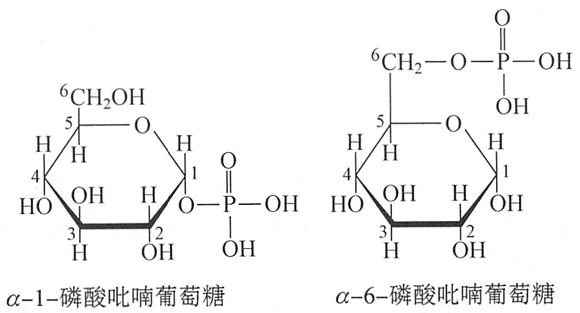
单糖的磷酸酯在生命过程中具有重要意义,它们是人体内许多代谢过程中的中间产物。例如, 1-磷酸吡喃葡萄糖及6-磷酸吡喃葡萄糖。 #生化
(二)成苷反应
单糖的半缩醛羟基与含羟基的化合物(如醇、酚等)作用,可脱去一分子水,生成糖苷(glycoside)。此反应称为成苷反应。例如:D-葡萄糖在无水酸(通常使用干燥HCI)催化下,与甲醇反应可生成D-葡萄糖甲苷(或甲基-D-葡萄糖苷)。
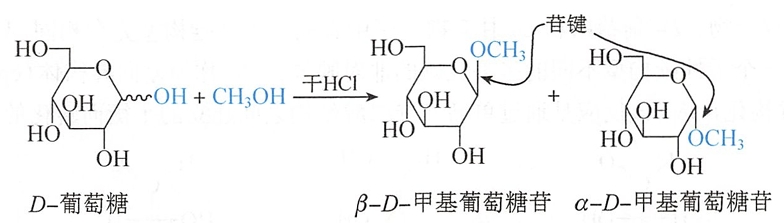
糖苷是由糖和非糖两部分组成。上述糖苷是由D-葡萄糖和甲醇通过氧苷键结合成苷。糖苷分子中无半缩醛羟基,不能通过互变异构转化成开链结构,故无变旋光现象。
与其他缩醛一样,糖苷键在碱性条件下稳定,在酸作用下很易水解,生成原来的糖和非糖部分。此外,酶对糖苷水解有专一性,例如杏仁酶专一性地水解β-糖苷,而麦芽糖酶只水解α-糖苷。
糖苷广泛分布于自然界中,很多具有生物活性。糖部分的存在可增加糖苷的水溶度。
(三)成脎反应
单糖与过量的苯肼一起加热作用,会生成难溶于水的黄色结晶物质,叫做糖脎(osazone)。糖脎的生成可分三个阶段进行。单糖先与苯肼作用生成苯腙,然后苯腙中原来与羰基相邻碳(醛糖的 C-2,酮糖的C-1)上的羟基,被苯肼氧化为新的羰基,它再与苯肼作用生成二苯腙,即糖脎。
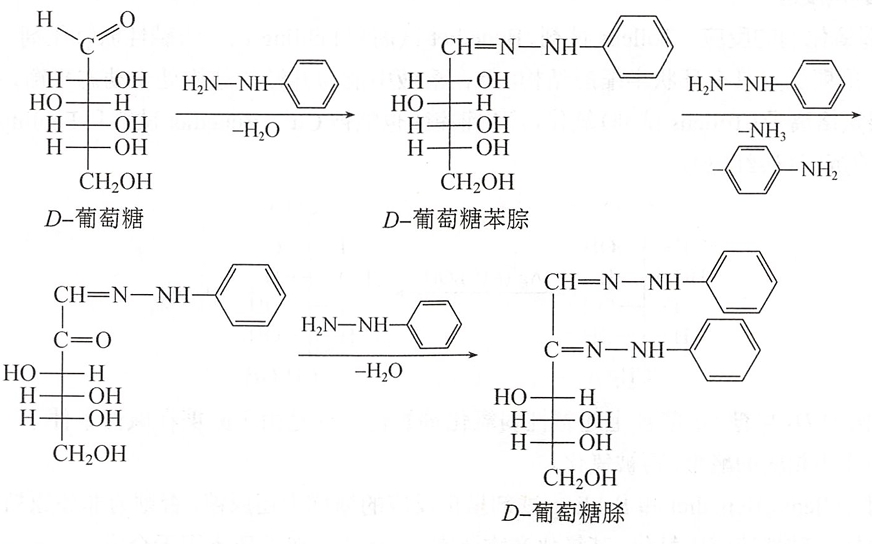
由于成脎反应只发生在单糖的C-1和C-2上,不涉及其他碳原子。因此,凡是碳原子数相同的单糖,除C-1,C-2外,其余手性碳原子构型完全相同时,都能生成相同的糖脎。例如,D-葡萄糖、D-甘露糖和D-果糖所生成的糖脎都一样。
不同的糖生成糖脎所需的时间不同。一般来说,单糖快些,二糖慢些。糖脎是难溶于水的黄色结晶,不同的糖脎具有不同的晶形和熔点。因此,常用糖脎来鉴别不同的糖。
(四)糖的差向异构化
反应用稀碱[如Ba(OH)2]的水溶液处理D-葡萄糖,经过数天放置后,就会得到D-葡萄糖、D-甘露糖和D-果糖的混合物。
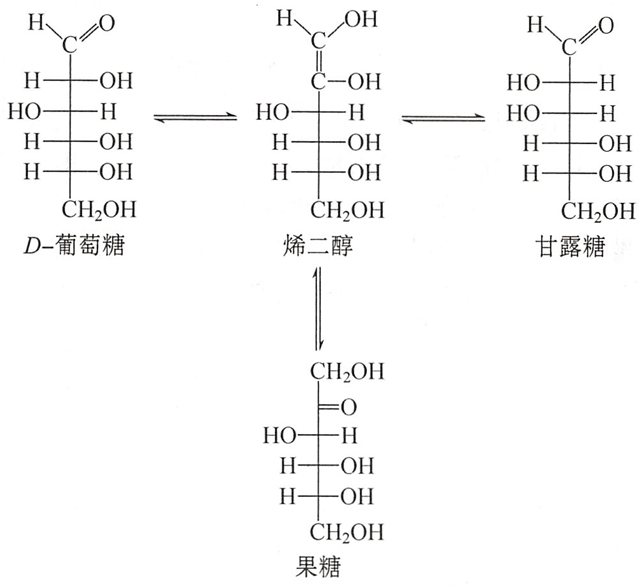
D-葡萄糖和D-甘露糖分子中有三个手性碳构型完全相同,只有一个手性碳不同,这种仅有一个手性碳构型不同的多手性碳的非对映异构体,称为差向异构体(epimer)。
这个过程被称为差向异构化反应,该反应是通过单糖和烯二醇结构之间建立的平衡而转化的。
(五)氧化反应
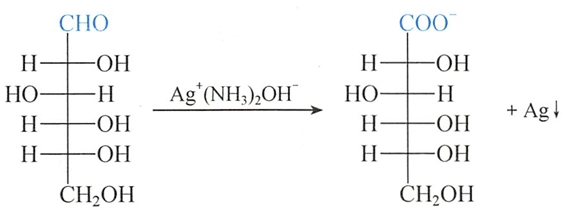
1.与弱氧化剂的反应
Tollens试剂、Benediet试剂和Fehling试剂为碱性弱氧化剂,能把醛基氧化成羧基。单糖虽然具有环状半缩醛结构,但在溶液中能与开链的结构处于动态平衡,所以开链的醛糖能被银氨络离子(Tollens试剂)氧化,产生银镜;也能被Cu2+(Benedict试剂和Fehling试剂)氧化产生Cu2O的沉淀(砖红色)。
酮糖(例如D-果糖)也能被上述碱性弱氧化剂氧化。这是由于酮糖在碱性条件下,通过差向异构化反应转变为相应的醛糖,再被氧化。
凡是对Tollens、Benedict和Fehling试剂呈正反应的糖称为还原糖,否则为非还原糖。单糖都是还原糖。
单糖在碱性溶液中氧化,其氧化产物通常是混合物,该性质不用于合成。
2.与溴水的反应
溴水可与醛糖发生反应,选择性地将醛基氧化成羧基。由于在酸性条件下(溴水pH=6.00)糖不发生差向异构化,因此溴水不氧化酮糖。
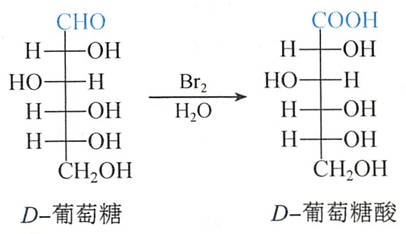
利用溴水氧化醛糖的性质可鉴别酮糖与醛糖。
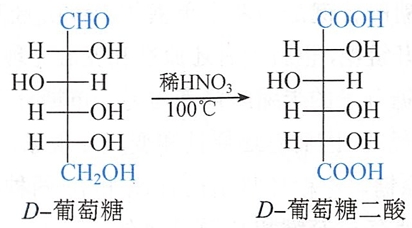
3.与稀硝酸的反应
硝酸是比溴水强的氧化剂。它不但可以氧化糖的醛基还可以氧化糖的伯醇羟基。生成二元羧酸,称为糖二酸。例如D-葡萄糖经硝酸氧化,生成D-葡萄糖二酸(glucaric acid)。
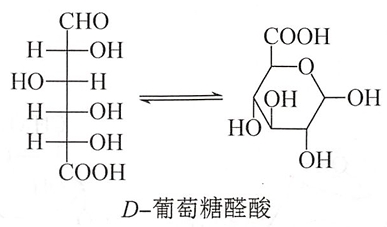
D-葡萄糖二酸经选择性还原,可得D-葡萄糖醛酸(glucuronic acid)。D-葡萄糖醛酸广泛存在于动物和植物体内。在动物肝脏中它可与某些有毒的醇、酚等物质结合,然后排出体外,从而起到解毒作用。 #生化
(六)酸性条件下的脱水反应
在弱酸条件下,含β-羟基的羰基化合物易发生脱水反应,生成α、β不饱和羰基化合物。糖类化合物具有上述结构特征,因此在酸性条件下易脱水生成二羰基化合物。
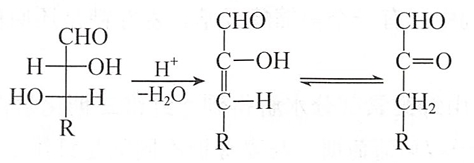
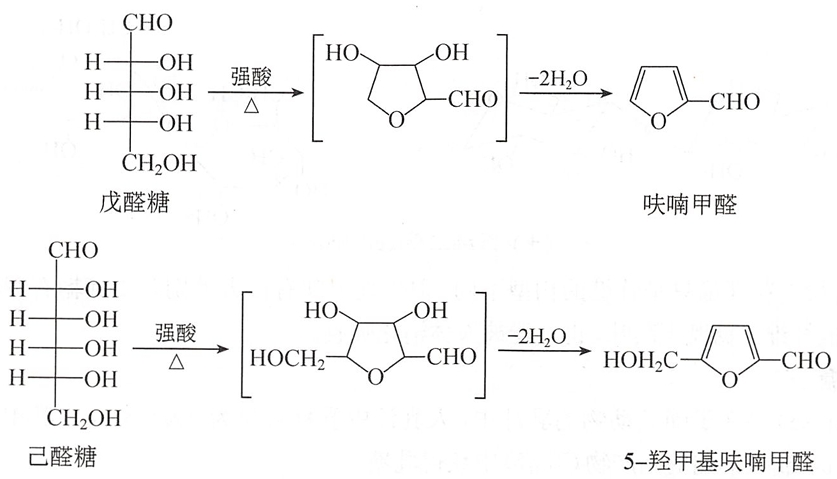
戊醛糖在强酸条件下(如12%HCl)加热,分子脱水生成呋喃甲醛。己醛糖在上述条件下则得到5-羟甲基呋喃甲醛。